熱力学って色んな過程があってよくわからないんだけど…


それじゃあ今回は系の状態変化のさせ方についてまとめてみよう。
本記事では熱力学の状態変化について解説します。
熱力学では、等圧過程やら断熱過程やらいろんな状態変化のさせ方がありますので、それぞれを復習していきましょう。
動画でも解説していますので、是非そちらも参考にしていただければと思います。
熱力学の考え方
まず、熱力学の考え方を復習しておきましょう。
熱力学ではたくさんの粒子などをまとめて系として扱うのですが、この系を状態変化を考える学問でした。
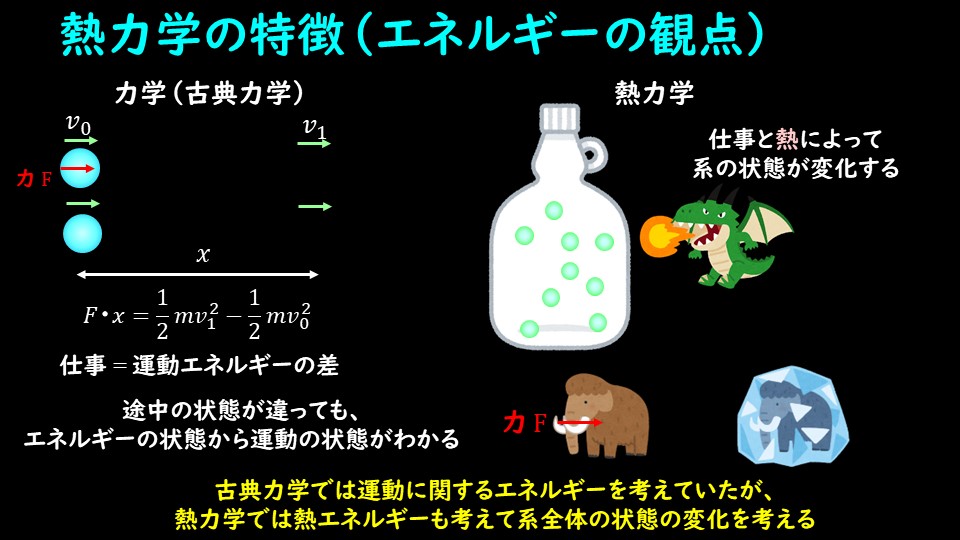
状態変化を考えるにあたって、変化の前後を考えて入ってきた熱や仕事を求める方法が、熱力学第一法則、エネルギー保存則でしたね。
熱力学第一法則を使えば、状態変化の変化の過程に関係なく、熱や仕事というものがもとまるのですが、
熱と力学的エネルギーと変数が2つあるわけです。
これらの熱エネルギーであったり、力学的エネルギーを何とかして求めたい!ということも当然あるわけで、
そのためには状態変化の経路の情報が必要となってくるわけですね。
その状態変化の経路が〇〇過程と呼ばれています。(等圧過程とか等積過程とか・・・)
というわけで様々な過程についてここから考えていきましょう。
キーとなるのは、状態方程式と熱力学第一法則です。
等圧過程
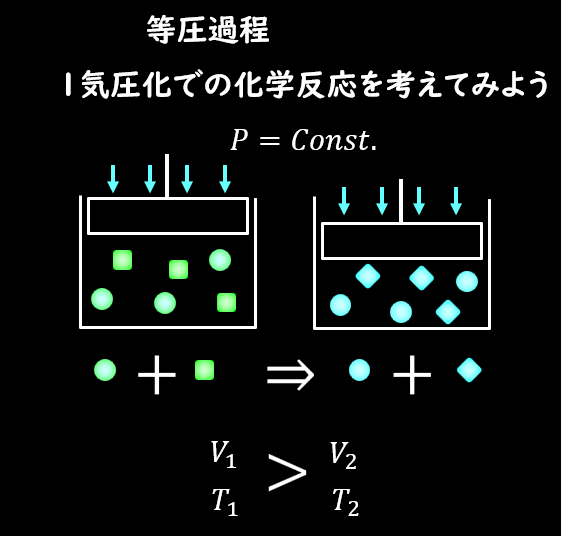
等圧という名の通り、圧力が一定の過程のことを等圧過程と呼びます。
ここで圧力といっても、外圧と内圧の2つがあるのですが、外圧を一定とすることが多いので外圧一定と考えるようにしましょう。
等圧過程の例としては、大気中の化学反応とかが等圧過程に相当します。
常に大気圧にさらされた状態だと、圧力は一定となりますね。
状態方程式を考えると、図中の体積\(V_1\)から\(V_2\)に小さくなったとすると、系の温度\(T_1\)は\(T_2\)へ参賀ることになります。
等積過程

等積過程は体積が一定の状況下での過程となります。
かた〜い容器の中に気体を入れて化学反応させると、容器の体積は変わらないので、等積過程となりますね。
等温過程
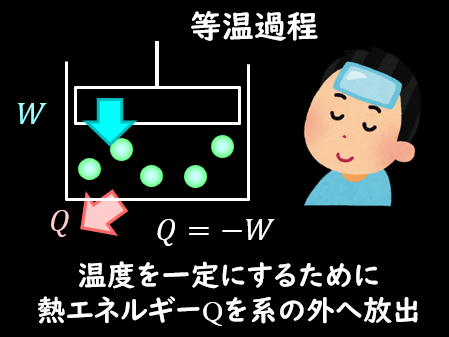
等温過程は、温度が一定の状況下での過程となります。
イメージとしては容器の温度を一定になるように、容器を水につけながら反応させたり、
発熱反応であれば、発熱した熱を吸収できるように冷えピタを貼ってみる、みたいな感じです。
断熱過程
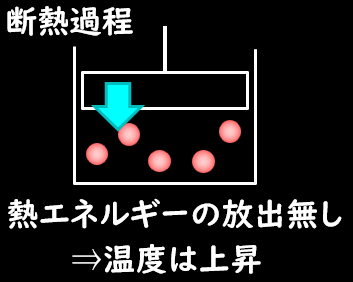
等温過程と間違いやすいのですが、熱の出入りが無い過程のことを断熱過程と呼びます。
断熱容器を用意して、力学的エネルギーを与えたり、取り去ったりするような過程です。
イメージとしては魔法瓶のように、熱の出入りがしにくい容器を持ってきて、ピストンで忍足引いたりすることで気体の状態変化をする感じです。
準静的過程
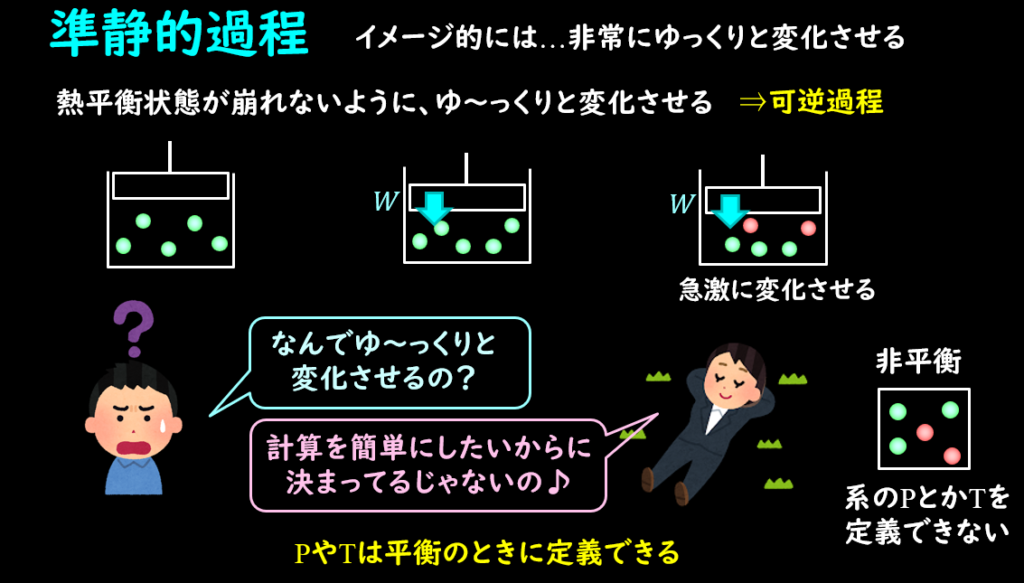
準静的過程は非常にゆっくりと状態変化させるような過程です。
急激に状態変化させると、熱や力学的エネルギーの他に、摩擦や音などエネルギーロスが生じることがあります。
そのようなエネルギーロスがあるとややこしくなるので、ゆっくりと変化させ、平衡状態を保ったまま変化させることを準静的過程と呼んでいます。
圧力や体積など特別な状態量を固定している過程ではなく、あくまで変化のスピードを示していると考えてください。
準静的に等圧過程で変化させる、などと言った時には、非常にゆっくり、等圧過程で変化させたんだなと思ってくださいね。
ちなみに非平衡の状態だと、系の圧力Pや温度Tなどの状態量を定義することが困難になりますので、注意しておきましょう。
まとめ
高校物理でもよく出てくる〇〇過程について、ざっと復習しました。
これらの過程を前提として、いろいろと状態を議論していくことになりますので、しっかりと過程のイメージできるようにしておきましょうね。
